
Ariceum: Studie mit Jod-123 zur PARP-Hemmung
Ariceum Therapeutics erhält in Großbritannien die Genehmigung zur Durchführung einer klinischen Phase I-Studie mit dem ersten Jod-123-markierten PARP-Inhibitor bei Patienten mit rezidivierendem Glioblastom.
Die Berliner Radiopharmafirma Ariceum Therapeutics hat in Großbritannien von der britischen Regulierungsbehörde für Arzneimittel und Gesundheitsprodukte (MHRA) die Genehmigung zur Durchführung einer klinischen Phase I-Studie (CITADEL-123) mit 123I-ATT001, einem Jod-123-markierten PARP-Inhibitor, bei Patienten mit rezidiviertem Glioblastom erhalten. Ariceum hatte im Dezember 2023 bei der MHRA einen Antrag auf Genehmigung einer klinischen Studie (Clinical Trial Authorisation, CTA) eingereicht. Die Phase I-Studie soll im Juni 2024 in Großbritannien beginnen.
Die Auswahl des strahlenden Isotops und der Beginn der klinischen Erprobung in Großbritannien sind kein Zufall. Der Wirkstoff mit Isotopenligand wurde urspprünglich von der britischen Theragnostics Ltd. entwickelt, die im Sommer 2023 von Ariceum für eine Upfrontzahlung von 2,5 Mio. US-Dollar und meilensteinbasierten möglichen weiteren rund 40 Mio. US-Dollar übernommen worden war. Das Jod-123 ist ein sogenannter Auger-Emittent, der nur im Nanometerbereich seine energiereiche Strahlung abgibt und damit für umgebendes Gewebe nahezu vollständig unschädlich ist. Die Herausforderung ist somit, diese Strahlung dorthin zu bringen, wo auch kleine Hochenergieladungen einen (gewollten) Schaden anrichten können: in die Zelle. Ariceum ist damit nun das erste Unternehmen, das eine klinische Studie zur Auger-Therapie durchführt, die auf das DNA-Reperaturenzym PARP (Poly-ADP-Ribose-Polymerase) abzielt. Bei Krebszellen gerät durch das enthemmte Wachstum die Reparaturmaschinerie der DNA-Replikation beständig ins Hintertreffen, es entstehen weitere Mutationen, die das Wachstum gegebenfalls sogar noch beschleunigen. Der Gedanke der Hemmung des Reperaturenzyms PARP gründet darauf, dass eine noch stärkere Schädigung wie auch DNA-Brüche die Krebszelle in den „Selbstmord“ treiben sollten.
Im Jahr 2014 wurde der erste derartige PARP-Inhibitor zugelassen, Olaparib von AstraZeneca. Seither sind drei weitere ähnlich wirkende Arzneimittel zugelassen worden, mehrere Wirkstoffe befinden sich in der klinischen Entwicklung. Ariceum/Theragnostics nutzt den Wirkstoff von AstraZeneca über eine Lizenz und startet seine klinische Erprobung bei rezidivierendem Glioblastom, einer aggressiven Hirntumorform.

 Nuclidium AG
Nuclidium AG Molecular Partners AG
Molecular Partners AG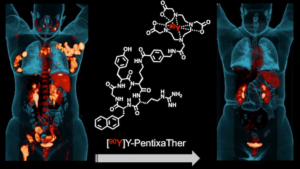 by the Society of Nuclear Medicine (Buck AK, Grigoleit GU, Kraus SK, Schirbel A, Heinsch M, Dreher N, Higuchi T, Lapa C, Hänscheid H, Samnick S, Einsele H, Serfling SE, Werner RA. C-X-C Motif Chemokine Receptor 4-Targeted Radioligand Therapy in Patients with Advanced T-Cell Lymphoma. J Nucl Med. 2022), Uniklinikum Würzburg
by the Society of Nuclear Medicine (Buck AK, Grigoleit GU, Kraus SK, Schirbel A, Heinsch M, Dreher N, Higuchi T, Lapa C, Hänscheid H, Samnick S, Einsele H, Serfling SE, Werner RA. C-X-C Motif Chemokine Receptor 4-Targeted Radioligand Therapy in Patients with Advanced T-Cell Lymphoma. J Nucl Med. 2022), Uniklinikum Würzburg